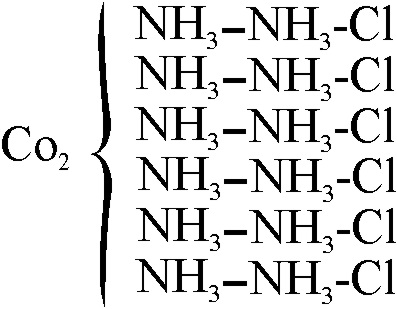
Fig.1
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
Simbología química 8: Nomenclatura inorgánica moderna.
La formulación Stock
La nomenclatura inorgánica tradicional de la escuela francesa encabezada por Lavoisier, no resultaba operativa, al descubrirse nuevos compuestos, pues los sufijos oso e ico, o ito y ato (sales), para diferenciar los compuestos no era suficiente. Cuando se trataba de nombrar compuestos complejos, presentaba enormes dificultades.
Los compuestos de cobalto con
valencia 2, en medio amoniacal, de diferentes colores, llamaron la atención
de los químicos de la segunda mitad del siglo XIX. Fremy ideó en 1852, una
manera de nombrarlos según el color. Así se conocía el cloruro de lúteo cobalto
(amarillo), el de práseo cobalto (verde), el roseocobaltico(rosa) etc. Se creían que todos tenían la fórmula Co2Cl6,
con cierta interacción con el disolvente(amoniaco), hay que tener en cuenta
que en aquella época solo se conocía el método de la densidad de vapor para
determinar los pesos moleculares. Hasta 1890, no se introdujo el término hexamino, para identificar al compuesto
[1]
. Una vez identificado que se trataba de una amina de cobalto
la fórmula del cloruro de lúteocobalto
se comienza a escribir como Co2Cl6.12NH3,
dando Blomstrand la fórmula de la fig. 1:
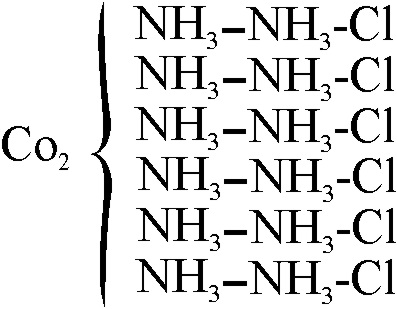
Fig.1
Los trabajos de Jorgensen y Peterson en Copenhague entre 1890 y 1892, comprueban que no se trata de un dímero y lo formulan como CoCl3.6NH3 . Pero había que explicar como se producía la unión con el NH3. Esto lo va a hacer el químico alemán Alfred Werner, profesor en el politécnico de Zurich, como el mismo dijo en una noche de inspiración [2] , proponiendo las valencias secundarias [3] , con las que el disolvente se coordinaría con el metal ; había nacido en 1892, la química de la coordinación. Por ello le dieron el Nobel de química de 1913.
Pero había que nombrar los nuevos compuestos, lo cual no era posible empleando la nomenclatura de Lavoisier.
A principios del siglo XX, hubo varios intentos de modificar la nomenclatura, empleando prefijos numéricos o letras para las valencias o los átomos de los elementos en determinados compuestos.
En 1902, Bohuslav Brauner, propone un sistema en el cual la valencia del elemento, se indicaría con un sufijo específico, como los que se indican en la tabla 1
| valencia |
sufijo |
| 1 |
a |
| 2 |
o |
| 3 |
i |
| 4 |
e |
| 5 |
an |
| 6 |
on |
| 7 |
in |
| 8 |
en |
De esa forma el KAg(CN)2, se denominaría dicianoargentate de potasio, mientras que el Na2S2O3, se llamaría tiotrioxosulfuronato de sodio y el K2PtCl6, hexacloroplatenato de potasio. Como se aprecia el sistema Brauner, es el primero en emplear prefijos numéricos y sufijos específicos, para indicar hasta 8 valencias, lo cual abarcaba mucho más que el sistema clásico de Lavoisier.
Rosenheim y Kopper, en 1909, hacen un primer intento de formulación sistemática, indicando el número de átomos de cada elemento que entran en una fórmula, así el óxido férrico Fe2O3, será:
3-óxido de 2-hierro
Este sistema fue muy criticado por Stock y Jordis. Stock, químico alemán, que había trabajado en la universidad de Berlín con Fischer, y posteriormente con Moissan en París, se dedicaba al estudio de los hidruros de boro, compuestos que no se podían formular a través del sistema tradicional, debido a la capacidad del boro a unirse consigo mismo, tal como los hidrocarburos e hidrosiluros.
En 1920, Werner publica la nueva nomenclatura para los complejos inorgánicos [4] .
Primero se nombra el anión y luego el catión como en la nomenclatura tradicional, pero los grupos coordinados, que Stock en 1916, llamó ligandos, antecederán al metal, con el siguiente orden:
1) grupos negativos (con el sufijo
o) : bromo, cloro, fluoro, nitro (NO2-), ciano (CN-)
oxo (O2-), peroxo( O2 2-) hidroxo
(OH-) etc.
2) Agua , empleando el término aquo
3) Derivados del amoniaco, empleando directamente los nombres de las aminas
4) Amoniaco, empleando el nombre ammina
Si hubiera varios ligandos, irían precedido del prefijo numérico correspondiente: di, tri, tetra etc.
Al metal que aparece en el catión, también se le agrega un sufijo para indicar su estado de oxidación, según la tabla 2, similar al sistema Brauner :
| nº
oxidación |
sufijo |
| 1 |
a |
| 2 |
o |
| 3 |
i |
| 4 |
e |
En complejos polinucleares, el ligando que actúa como puente vendrá precedido de la letra griega :.
Este sistema fue adoptado por Stock en 1920, y Delepine publica en 1926, la reforma de la nomenclatura inorgánica, resumen de los acuerdos de la Comisión de la Unión Internacional de Química (I.U.C), donde se introducen el número de oxidación del metal con números romanos. La comisión otra vez con el nombre de IUPAC (Unión internacional de Química pura y aplicada) realiza algunas modificaciones sobre la nomenclatura Werner-Stock, refrendándolas en 1940.
Así, se pueden observar las modificaciones que sufrió el CoCl3.6NH3 en la tabla 3
| Jorgensen,
1892 |
Cloro
amina de cobalto |
| Werner,
1920 |
Cloruro
de hexammincobáltico |
| Delepine,
1926 |
Cloruro
de hexammin-cobalto (III) |
| IUPAC,
1940 |
Cloruro
de hexammincobalto(III) |
Stock, aplica la nomenclatura
de complejos, a los compuestos inorgánicos binarios, ternarios y cuaternarios,
considerando que el oxígeno, actúa como un grupo oxo, con número de oxidación
2- (ver tabla 4)
| |
Compuesto |
Nombre
Stock |
| 1 |
FeO |
Óxido
de hierro(II) |
| 2 |
Fe2O3 |
Óxido
de hierro(III) |
| 3 |
Fe3O4 |
Óxido
doble de hierro(II) y (III) |
| 4 |
CrO3 |
Óxido
de cromo(VI) |
| 5 |
PbO2 |
Óxido
de plomo(IV) |
| 6 |
Pb3O4 |
Óxido
doble de plomo(II) dímero y (IV) |
| 7 |
ClO2 |
Óxido
de cloro(IV) |
| 8 |
Cl2O6 |
Óxido de dimero de cloro(VI) |
| 9 |
NO2 |
Óxido
de nitrógeno(IV) |
| 10 |
N2O4 |
Óxido de dímero de nitrógeno(IV) |
Naturalmente el problema surge para distinguir los peróxidos,
u óxido peróxidos, así el Na2O2, no se puede nombrar
como óxido de sodio(II), sino como peróxido de sodio. Si hubiera sobre un
mismo metal, varios grupos oxo y peroxo, se nombrarían alfabéticamente precedidos
del prefijo numérico que lo indique.
El sistema Werner-Stock, era un sistema de la escuela alemana. Stock que era el presidente de la comisión alemana para la nomenclatura química, tenía graves problemas de salud, por un envenenamiento con mercurio, producido por respirar durante muchos años los vapores de mercurio, al trabajar con los hidruros de boro a baja presión. La guerra destruye su laboratorio y sus posesiones, y hace que se retire a Aken, en la orilla del Elba, donde moriría el 12 de agosto de 1946 [5] .
Al terminar la guerra mundial,
con Alemania ocupada, sus químicos dispersos, y los que habían quedado en
su país impedidos de realizar investigaciones, los vencedores dictan las normas.
No es de extrañar que en 1949, los químicos ingleses Ewens y Basset, quisieran transformar el sistema Stock, empleando
en vez de números romanos, los arábigos seguidos del signo de la carga, así
en la tabla 5, se pueden ver ejemplos de dicha transformación:
| |
Compuesto |
Stock-Werner |
Ewens-Basset |
| 1 |
FeO |
Óxido
de hierro(II) |
Óxido
de hierro(2+) |
| 2 |
Fe2O3 |
Óxido
de hierro(III) |
Óxido
de hierro(3+) |
| 3 |
Fe3O4 |
Óxido
doble de hierro(II) y (III) |
Óxido
doble de hierro(2+) y (3+) |
| 4 |
CrO3 |
Óxido
de cromo(VI) |
Óxido
de cromo(6+) |
| 5 |
PbO2 |
Óxido
de plomo(IV) |
Óxido
de plomo(4+) |
| 6 |
ClO2 |
Óxido
de cloro(IV) |
Óxido
de cloro(4+) |
| 7 |
NO2 |
Óxido
de nitrógeno(IV) |
Óxido
de nitrógeno(4+) |
El sistema Ewens-Basset no prevaleció [6] , aunque su expresión del número de carga iónica se emplea todavía en muchos compuestos.
En 1953, la
IUPAC, edita las Tentatives Rules,
un intento de generalizar el sistema Stock-Werner, introduciendo algunas modificaciones
importantes, que no fueron refrendadas hasta la conferencia de París de 1957.
Las reglas del 57, desaconsejaban el uso de los sufijos oso e ico, para indicar
los estados de oxidación inferior y superior de los elementos, recomendando
el sistema Stock, para indicar el estado de oxidación con numeración romana,
o incluso con el arábigo de Ewens-Basset.
Introducen nombres específicos para los diferentes hidruros de los no metales
(silano, fosfina, arsina, estibina etc), y suprimen los anhídridos y óxidos
del nitrógeno con todos sus sufijos. También prohiben el prefijo bi, para
sales ácidas, que deberán llevar el término hidrógeno antepuesto al nombre
del anión, para indicar el hidrógeno sustituible presente
[7]
. En el caso de existir varios se indicaría con un prefijo
numérico unido al término hidrógeno. Al año siguiente se edita la primera
edición del libro rojo, donde estas reglas se reafirman.
Posteriormente
la IUPAC, edita en el 1965, la revisión de las reglas anteriores introduciendo
algunas nuevas realmente importantes, que no sólo afectaban a la formulación
[8]
. En la formulación tradicional se revisa y simplifica la
nomenclatura de sales dobles y triples, introduciendo el orden alfabético
tanto en aniones por los que se inicia, como en los cationes.
Los compuestos
dobles o triples se nombrarían alfabéticamente, primero los aniones que hubiera
y luego los cationes. Los ejemplos se ven en la tabla 6
| |
Nombre |
Fórmula |
| 1 |
Óxido
doble de hierro (II) y titanio(IV) |
FeTiO3 |
| 2 |
Hidróxido
triple de aluminio, potasio y
sodio |
KNaAl(OH)5 |
| 3 |
Cloruro
difluoruro de sodio |
Na3ClF2 |
| 4 |
Nitrato
de sodio y talio(I) |
NaTl(NO3)2 |
| 5 |
Cloruro
hidróxido de magnesio
[9]
|
Mg(OH)Cl |
Estos compuestos se formularían, sumando matemáticamente las formas individuales, e introduciendo los subíndices necesarios, partiendo de la neutralidad eléctrica como se indica en la figura 2. Solo se indicará la valencia del catión en caso de necesidad, por ser polivalente el elemento en cuestión. Ahora bien mientras se nombra alfabéticamente, se escribe en función de su electronegatividad aproximada, de menos a mas.
En esta revisión
saldrá reforzada la formulación Stock-Werner que se adaptará a todo tipo de
compuestos.
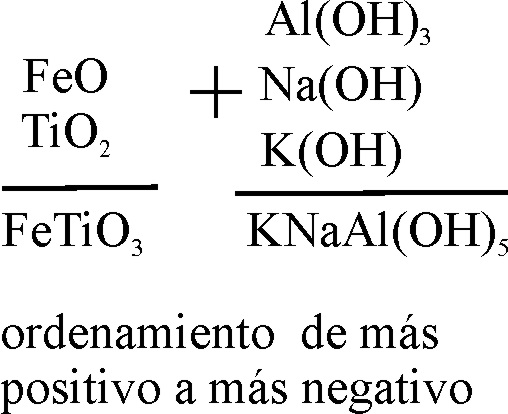
Fig.2
El sistema Stock-Werner se extendió a los compuestos ternarios y cuaternarios, considerando a los oxígenos como ligandos oxo [10] del metal correspondiente, con el sufijo ato, para los aniones, en cualquier estado de oxidación en el que se encuentre, indicando con un prefijo numérico el número de grupos oxo, que lo rodean. En el caso de que hubiera diferentes ligandos que afecten al anión, se nombrarán alfabéticamente sin tener en cuenta el prefijo numérico (tal como en la nomenclatura orgánica). El catión o los cationes se nombrarán alfabéticamente precedidos de la preposición de y seguidos del estado de oxidación, si fuera necesario, y sin tener en cuenta los prefijos numéricos que hubiera. Como prefijos multiplicativos, los griegos latinizados [11] que indican el 2,3,4,5 y 6, y no se indica el 1.
Por ese motivo esta nomenclatura
introduce el principio de construcción molecular, que más tarde se desarrollará.
Veamos ejemplos en la tabla 7:
| |
Compuesto |
Nombre Stock-Werner |
| 1 |
K2CuO2 |
Dioxocuprato(II)
de potasio |
| 2 |
Na
Al(OH)4 |
Tetrahidroxoaluminato(III)
de sodio |
| 3 |
K2CrO4 |
Tetraoxocromato(VI)
de potasio |
| 4 |
K2Cr2O7 |
Heptaoxodicromato(VI)
de potasio |
| 5 |
KMnO4 |
Tetraoxomanganato(VII)
de potasio |
| 6 |
K5IO6 |
Hexaoxoyodato(VII)
de potasio |
| 7 |
H2SO3(O2) |
Trioxoperoxosulfato(VI)
de hidrógeno |
| 8 |
H2S2O3 |
Trioxotiosulfato(VI)
de hidrógeno |
| 9 |
K3AsOS3 |
Oxotritioarseniato(V)
de potasio
[12]
|
| 10 |
Fe2(SO3)3 |
Trioxosulfato(IV) de hierro(III) |
| 11 |
Fe2(SO4)3 |
Trioxosulfato(VI) de hierro(III) |
| 12 |
Pb3(PO4)4 |
Tetraoxofosfato(V) de plomo
(IV) |
| 13 |
Ca(ClO4)2 |
Tetraoxoclorato(VII)
de calcio |
| 14 |
Al(NO2)3 |
Dioxonitrato
de aluminio |
| 15 |
Ca(HCO3)2 |
Hidrógenotrioxocarbonato(IV)
de calcio |
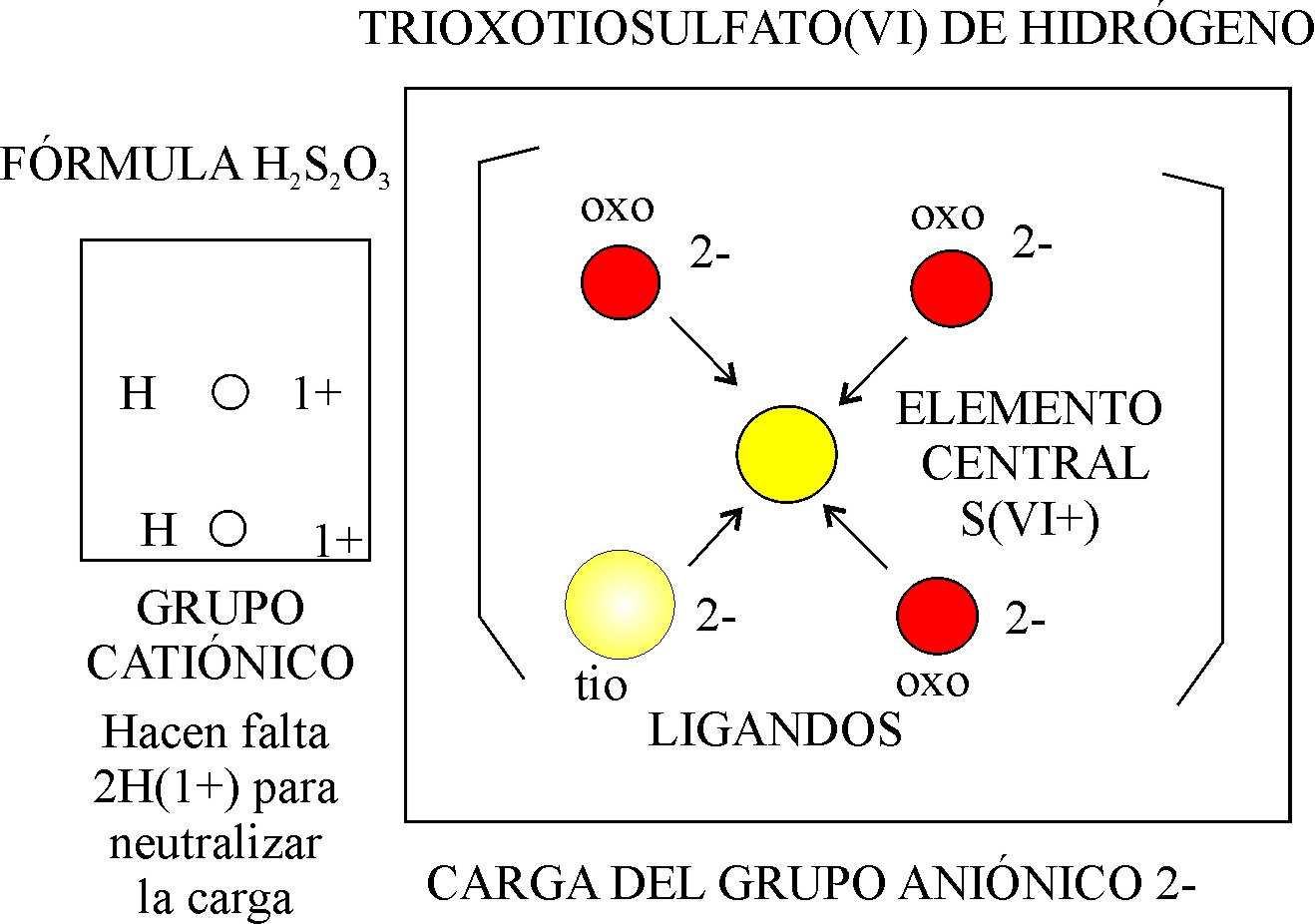
Fig.3
Realmente el mecanismo de formulación Stock-Werner es muy fácil. Vamos a aplicarlo al ejemplo 8 de la tabla anterior (fig. 3) el trioxotiosulfato(VI) de hidrógeno (no hace falta indicar dihidrógeno, ya que el principio de electroneutralidad, así lo exige) [13] .
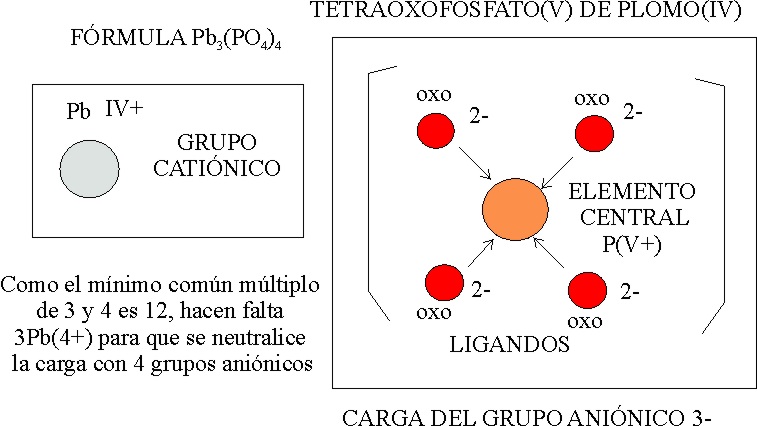
Fig.4
En el caso de una sal se operaría del mismo modo. Así en el ejemplo 12. Como se aprecia, en la fig.4 siguiendo el principio de neutralización de las cargas, en el supuesto que el grupo oxo, actúa como 2-, se establece la carga del anión que deberá ser neutralizada por la del catión, lo cual implica un intercambio de los superíndices al pasar a subíndices.
| |
Compuesto |
Nombre Stock-Werner funcional |
| 1 |
HClO |
Ácido
óxoclórico(I) |
| 2 |
HClO2 |
Ácido
dioxoclórico(III) |
| 3 |
HClO3 |
Ácido
trioxoclórico(V) |
| 4 |
HClO4 |
Ácido
tetraoxoclórico(VII) |
| 5 |
H2SO3 |
Ácido
trioxosulfúrico(IV) |
| 6 |
H2SO4 |
Ácido
tetraoxosulfúrico(VI) |
| 7 |
H2CrO4 |
Ácido
tetraoxocrómico(VI) |
| 8 |
H2Cr2O7 |
Ácido
heptaoxodicrómico(VI) |
| 9 |
HMnO4 |
Ácido
tetraoxomangánico(VII) |
| 10 |
H5IO6 |
Ácido
hexaoxoyódico(VII) |
| 11 |
H2SO3(O2) |
Ácido
trioxoperoxosulfúrico (VI) |
| 12 |
H2SO2(O2) |
Ácido
trioxoperoxosulfúrico (IV) |
| 13 |
H2S2O3 |
Ácido
trioxotiosulfúrico (VI) |
| 14 |
H3AsO4 |
Ácido tetraoxoarsénico(V) |
| 15 |
H3AsS2O2 |
Ácido
dioxoditioarsénico (V) |
Paralelamente al sistema Stock, la IUPAC elaboró otro sistema simplificatorio, indicando el número de átomos o grupos que intervienen en una fórmula, este sistema se denominó composicional o estequiométrico, porque indicaba directamente las relaciones interatómicas.
Comenzó a fraguarse al sustituir el término dímero empleado por Stock, por el prefijo di, para indicar dos, de esta forma algunos compuestos que tenían verdadera dificultad para nombrarse como los ejemplos 6 y 10 de la tabla 4 ( véase la tabla 9)
| |
Compuesto |
Nombre Stock |
Modificación |
| 6 |
Pb3O4 |
Óxido doble de plomo(II) dímero y (IV) |
Óxido doble de diplomo(II) y plomo(4) |
| 10 |
N2O4 |
Óxido de dímero
de nitrógeno(IV) |
Óxido de dinitrógeno(IV) |
| |
De átomo |
De
grupo |
| 2 |
di |
bis |
| 3 |
tri |
tris |
| 4 |
tetra |
tetraquis |
| 5 |
penta |
pentaquis |
| 6 |
hexa |
hexaquis |
| 7 |
hepta |
heptaquis |
| 8 |
octa |
octaquis |
| 9 |
nona |
nonaquis |
| 10 |
deca |
decaquis |
El prefijo mono, indicando 1, suele omitirse. Este sistema tiene el inconveniente de no indicar ni la estructura ni el estado de oxidación del elemento, se deberá escribir como se nombra, aunque de izquierda a derecha.
La introducción de los prefijos para grupos permitió completar la nomenclatura de los compuestos dobles o triples dentro de la nomenclatura tradicional, así en la tabla 11
| |
Nombre tradicional |
Fórmula |
| 1 |
Cloruro-fluoruro-bis(sulfato)
de sodio
[14]
|
Na6ClF(SO4)2 |
| 2 |
Cloruro-tris(nitrato)
de calcio |
Ca2Cl(NO3)3 |
| 3 |
Dicloruro-tetraquis(hidrógeno
sulfato) de magnesio |
Mg3Cl2(HSO4)4 |
Pero también crear la llamada
nomenclatura estequiométrica o composicional, que aplicada a los compuestos
de la tabla 6 y 7, se nombrarían conforme se indica en la tabla 12
| |
Compuesto |
Nomenclatura
estequiométrica |
| 5.1 |
FeO |
Óxido
de hierro |
| 5.2 |
Fe2O3 |
Trióxido
de dihierro |
| 5.3 |
Fe3O4 |
Tetraóxido
de trihierro |
| 5.4 |
CrO3 |
Trióxido
de cromo |
| 5.5 |
PbO2 |
Dióxido
de plomo |
| 5.6 |
ClO2 |
Dióxido
de cloro |
| 5.7 |
NO2 |
Dióxido
de nitrógeno |
| 6.1 |
K2CuO2 |
Dioxocuprato
de dipotasio |
| 6.2 |
Na
Al(OH)4 |
Tetrahidroxoaluminato
de sodio |
| 6.3 |
K2CrO4 |
Tetraoxocromato
de dipotasio |
| 6.4 |
K2Cr2O7 |
Heptaoxodicromato
de dipotasio |
| 6.5 |
KMnO4 |
Tetraoxomanganato
de potasio |
| 6.6 |
K5IO6 |
Hexaoxoyoadato
de pentapotasio |
| 6.7 |
H2SO3(O2) |
Trioxoperoxosulfato
de dihidrógeno |
| 6.8 |
H2S2O3 |
Trioxotiosulfato
de dihidrógeno |
| 6.9 |
K3AsOS3 |
Oxotritioarseniato
de tripotasio |
| 6.10 |
Fe2(SO3)3 |
Tris-Trioxosulfato de dihierro |
| 6.11 |
Fe2(SO4)3 |
Tris-Tetraoxosulfato de dihierro |
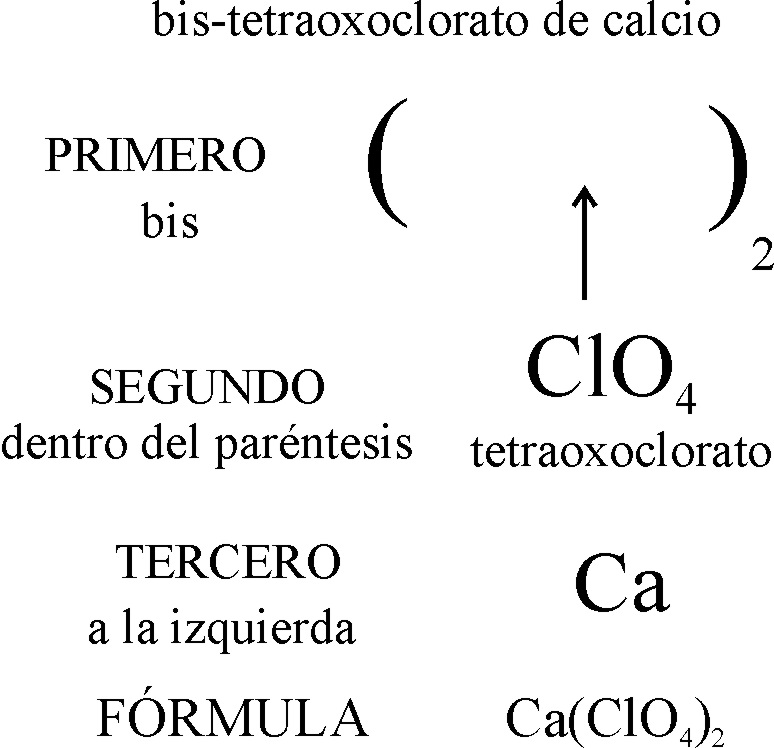
| 6.12 |
Pb3(PO4)4 |
Tetraquis-Tetraoxofosfato de
triplomo |
| 6.13 |
Ca(ClO4)2 |
Bis-Tetraoxoclorato
de calcio |
| 6.14 |
Al(NO2)3 |
Tris-Dioxonitrato
de aluminio |
| 6.15 |
Ca(HCO3)2 |
Bis-Hidrógenotrioxocarbonato
de calcio |
El grupo de la IUPAC, dirigido por Fernelius en 1971, en la segunda edición del libro rojo, introduce modificaciones en la nomenclatura tradicional, que afectaba a los ácidos del fósforo.
Efectivamente los ácidos del fósforo que se han visto nombrados desde mediados del siglo XVIII, por Graham (véase en DFQ13, SimbQ2 , en esta misma web [15] ), ya habían sufrido algunas modificaciones (tabla 13)
| |
Fórmula clásica |
Nombre clásico 1830 |
Nombre clásico modificado |
2ª Edición del libro rojo 1971 |
Formula modificada |
| 1 |
H3PO2 |
Ácido hipofosforoso |
|
Ácido fosfínico |
HPO2H2 |
| 2 |
HPO2 |
Ácido metafosforoso |
|
|
|
| 3 |
H4P2O5 |
Ácido pirofosforoso |
Ácido difosforoso |
Ácido difosfónico |
H2P2H2O5 |
| 4 |
H3PO3 |
Ácido ortofosforoso |
Ácido fosforoso |
Ácido fosfónico |
H2PHO3 |
| 5 |
HPO3 |
Ácido metafosfórico |
|
|
|
| 6 |
H4P2O5 |
Ácido pirofosfórico |
Ácido difosfórico |
|
|
| 7 |
H3PO4 |
Ácido ortofosfórico |
Ácido fosfórico |
|
|
El motivo de esta nueva propuesta, era su comportamiento. Efectivamente el ácido hipofosforoso sólo sustituía un H de los 3 que presentaba, y los ortofosforoso y difosforoso, sólo lo hacían 2 H, eso era anómalo y había que diferenciarlo en la nomenclatura.
Sin embargo muchos de estos
criterios serán modificados por la IUPAC, a partir del año 1999, introduciéndose
en el siglo XXI, una nueva nomenclatura, como se verá.
[1]
Es la primera
especie inorgánica con prefijo numérico, junto con la que se empleaba
para el K4Fe(CN)6, (hexaciano) conocido desde
hace mucho tiempo.
[2]
En unas charlas
con su colega Paul Pfeiffer le dijo Una madrugada, me desperté a las 2, se había hecho la luz en mi cerebro,
me puse a trabajar y a las cinco de la tarde la teoría de la coordinación
estaba resuelta.
[3]
Realmente Werner
no las llamó valencias secundarias , sino Nebenvalenzformel, algo así como fórmulas de valencia auxiliar.
[4] La publicación Contribución a la constitución de las combinaciones inorgánicasse hace después de muerto Werner que fallece en 1919. Previamente había realizado otra sobre nomenclatura, en 1916.
[5]
Es curioso el
paralelismo entre Werner y Stock, ambos Alfred. El primero nació en
una zona francesa , la Alsacia, que luego sería alemana. El segundo
en una zona alemana (Prusia), que posteriormente sería polaca (Gdansk)
[6]
Sin embargo
actualmente se emplea en bastantes ocasiones
[7]
Al no indicar nada más, se tomó de muy diversas formas
según los países, unos ,, lo mas, lo unieron
al anión, otros como la Chemical Society inglesa, lo separaron
del mismo
[8]
En las normas
del 65, se cambian los términos lantánidos y actínidos, por lantanoides
y actinoides, para los elementos 4f y 5f. Se suprime el término metaloide,
considerando los elementos en metales, no metales y semimetales. Define
el número de oxidación, con un número seguido del signo de la carga
y no al revés. Define las posiciones del número másico A
y el número atómico Z, como superíndices y subíndices a la izquierda
del símbolo del elemento y recomienda el uso de prefijos, para indicar
las formas alotrópicas de un elemento, así O2 será dioxígeno
y O3 el trioxígeno (lo cual motivará gran controversia, al
descartar el nombre de ozono, teniendo en cuenta que en química orgánica
se usaba, en los ozónidos y en la ozonólisis).
[9]
Este compuesto
también se podría formular como una sal básica, según las reglas de
la IUPAC, nombrándose como hidroxicloruro de magnesio
[10]
En inglés se
emplea el óxido en vez del oxo.
[11] También generó polémica, dado que el término valencia era latino y el tri y tetra eran griegos.
[12]
El número de oxidación
(en romano), se puede calcular fácilmente, teniendo en cuenta las reglas
de Werner publicadas en 1920, dado que la suma de las cargas deberá
se 0, así por en el ejemplo 9, K(1+), As(x), O(2-) S(2-). Por lo tanto si consideramos x la
carga del As, tendremos: 3(+1)+x+(-2)+3(-2)=0; x=+5
[13]
Obsérvese que
se sigue escrupulosamente el orden alfabético sin tener en cuenta los
prefijos numéricos.
[14]
En una nomenclatura
alternativa, se podrían indicar el número de cationes intervinientes,
con lo cual se convertiría en una nomenclatura estequiométrica : cloruro-fluoruro-bis(nitrato)
de hexasodio
[15]
Recuérdese que
los prefijos meta, piro y orto no significan 1, 2 y 3 moléculas de agua,
sino : el otro ácido, el ácido que se obtiene calentando y el ácido normal. Con anterioridad a Graham (1833),
se había empleado el prefijo piro, aplicándolo a ácidos orgánicos obtenidos
por la acción del calor. En 1834, Pelouze emplea el prefijo meta, para
nombrar a un ácido metagálico, y Liebig, opinaba que el prefijo meta
sólo se debería aplicar a los ácidos que tuvieran isómeros. En 1859,
Odling publica en el Philophical Magazine, un trabajo en el que se considera
ya a los ortofosfatos, como los compuestos ordinarios de fósforo, y
como se podían obtener a partir de los metafosfatos.