
Fig.8
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
PRECIPITACIÓN DE SALES DE Ag1+
7. Nitrato de plata y sulfuro
sódico. Solubilización del precipitado con disolución de hidróxido amónico.
Partimos de 2 gotas de nitrato de plata e sulfuro sódico disuelto en agua
(fig.1). Las unimos (fig.2). Rápidamente
se produce un precipitado oscuro de Ag2S (Kps=8.10-51),
que se extiende a las dos gotas (fig.2-3-). Pasado cierto tiempo el precipitado
comienza a formar estructuras arborescentes (fig.4-6) por formación de sulfuro
de plata marrón oscuro. Al agregar al precipitado hidróxido amónico
parcialmente se solubiliza, por formación del complejo amoniacal del ion
plata(I). (Fig.6-8)
El proceso que tiene lugar es:
AgNO3 (ac)+ Na2S (ac)= Ag2S(s)+ 2NaNO3
Precipitado pardo
negruzco
Ag2S(s)+4NH4.OH=[Ag(NH3)2] 2S+4H2O

Fig.8

Fig.7
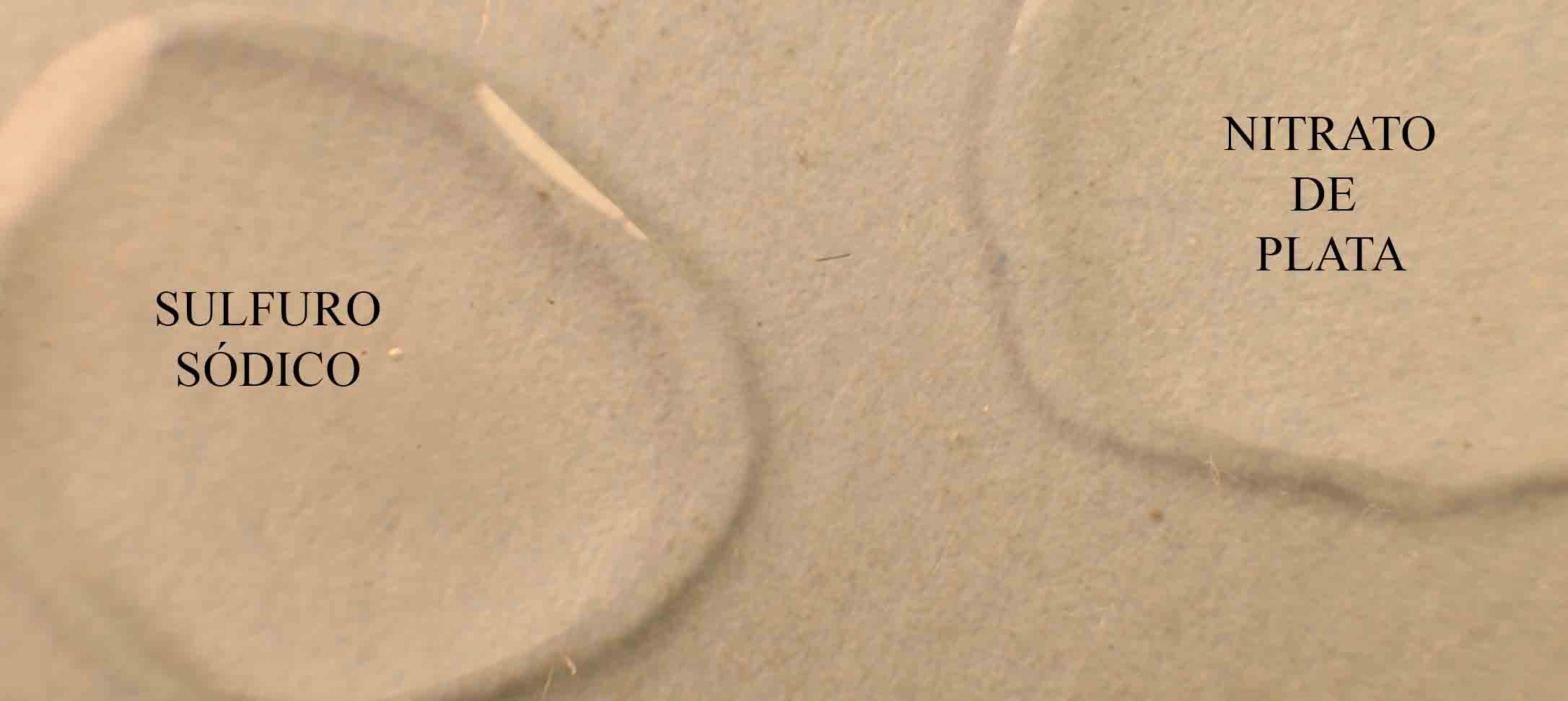
Fig.1
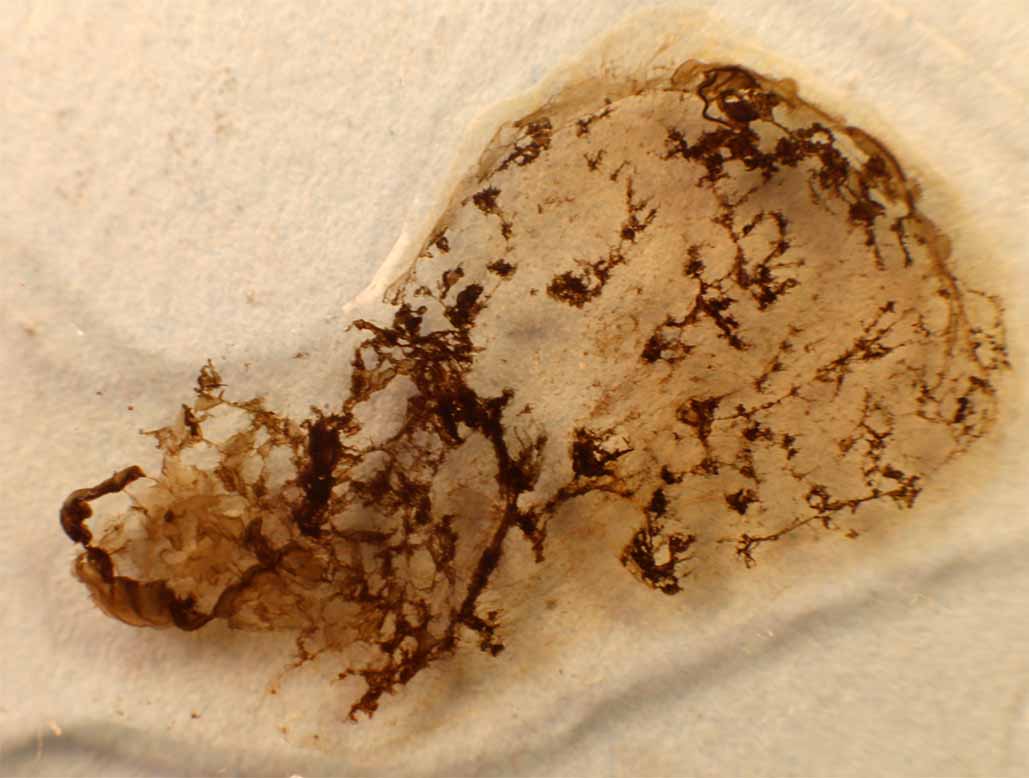
Fig.5
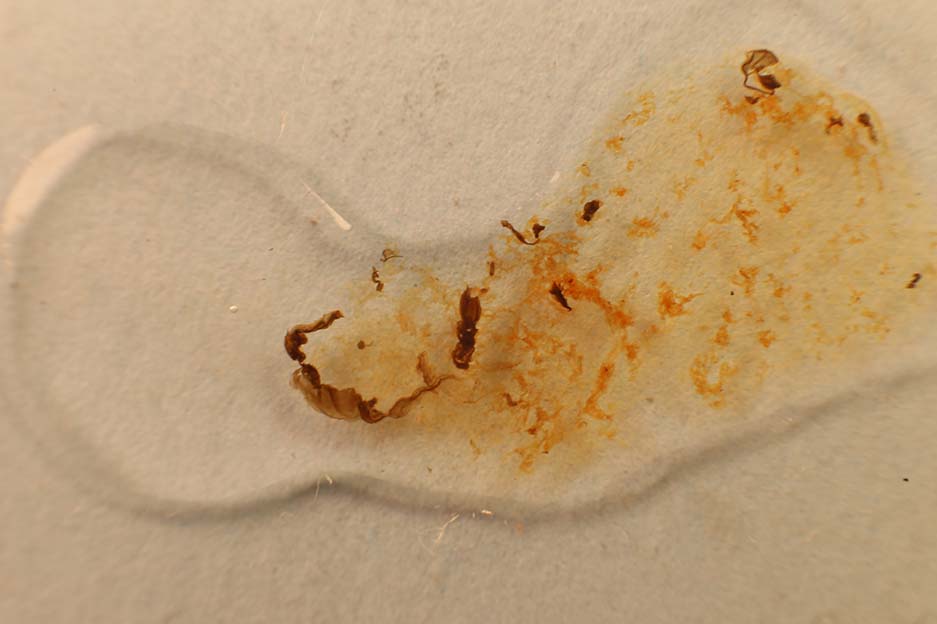
Fig.4

Fig.2

Fig.3

Fig.9

Fig.6